Merit Medical HepaSphere Microspheres(With Doxorubicin) IFU-Int'l User Manual
Page 40
välineen eheyden ja johtaa toimintahäiriöön. Tämä voi puolestaan johtaa
potilaan loukkaantumiseen, sairastumiseen tai kuolemaan. Uudelleen
käyttäminen, käsitteleminen tai sterilointi voi myös aiheuttaa väilneen
kontaminaatiovaaran ja infektion tai risti-infektion potilaalle, mm.
infektiotaudin/-tautien siirtymisen potilaasta toiseen. Välineen
kontaminaatio voi johtaa vaurioon, sairauteen tai potilaan kuolemaan.
Kaikki toimenpiteet tulee tehdä hyväksyttyä aseptista tekniikkaa
käyttäen.
HepaSphere-mikropalloja EI SAA käyttää niiden alkuperäisessä
kuivassa olomuodossa. Ne on sekoitettava käyttövalmiiksi ennen
käyttöä. HepaSphere-mikropallot turpoavat vesipitoisessa liuoksessa.
Turpoamisen voimakkuus riippuu liuoksen ionikonsentraatiosta.
Mikropallot turpoavat noin nelinkertaisiksi 0,9-prosenttisessa NaCl-
vesiliuoksessa ja non-ionisissa varjoaineissa alkuperäiseen kuivan
olomuodon läpimittaan verrattuna. Doksorubisiini-HCl:lla lastattujen
mikropallojen turpoamisen voimakkuus riippuu lastatun lääkeaineen
määrästä.
Kylmäkuivattu
doksorubisiini-HCl
täytyy
sekoittaa
käyttövalmiiksi 0,9-prosenttiseen NaCl-liuokseen. HepaSphere-
mikropallojen koko pienenee hieman, noin 20 %, doksorubisiini-HCl:lla
lastattuina verrattuna niiden kokoon pelkässä 0,9-prosenttisessa NaCl-
vesiliuoksessa. HepaSphere-mikropallot ovat kokoonpuristuvia, ja ne
voidaan injisoida helposti mikrokatetrien läpi. HepaSphere-mikropallojen
injisointi ennen niiden täydellistä turpoamista voi kuitenkin johtaa siihen,
ettei aiottua embolisaatiokohdetta tavoiteta, sekä mahdolliseen
laajemman kudosalueen embolisaatioon.
Huomautus: Doksorubisiini-HCl:n suositeltu enimmäiskonsentraatio on
5 mg/ml. Pitoisuuden 5 mg/ml ylittävät doksorubisiini-HCl-
konsentraatiot lisäävät merkittävästi liuoksen viskositeettia ja tekevät
liuoksesta hankalasti käsiteltävää HepaSphere-mikropallojen suhteen.
Ennen embolisaatiota saatetaan tarvita kortikosteroidien käyttöä niille
potilaille, joilla on todettuja allergioita non-ionisille varjoaineille.
Lisäarviot tai varotoimenpiteet voivat olla tarpeen toimenpiteen
yhteydessä annettavan hoidon toteuttamisessa niille potilaille, joilla on
seuraavia häiriöitä:
• Vuototaipumus tai hyperkoagulaatiotila
• Immuunijärjestelmän häiriö
MAHDOLLISET KOMPLIKAATIOT:
Verisuonten embolisaatio on suuria riskejä sisältävä toimenpide.
Komplikaatioita voi ilmetä koska tahansa toimenpiteen aikana tai sen
jälkeen ja niihin kuuluvat mm.:
• Halvaantuminen, joka johtuu kohdistamattomasta embolisaatiosta tai
viereisen kudoksen turvotuksen myötä syntyvästä iskeemisestä
vauriosta
• Ei-toivottu
HepaSphere-mikropallojen
takaisinvirtaus
tai
kulkeutuminen normaaleihin, kohdeleesion vieressä oleviin valtimoihin
tai leesion läpi muihin valtimoihin tai valtimoverkostoihin, kuten
sisempään
kaulavaltimoon,
keuhkoverenkiertoon
tai
sepelvaltimoverenkiertoon.
• AV-suntista johtuva keuhkoembolia
• Iskemia ei-toivotussa kohdassa, mukaan lukien iskeeminen
aivohalvaus, iskeeminen infarkti (sydäninfarkti mukaan luettuna) ja
kudosnekroosi
• Kapillaariverkoston okkluusio ja kudosvaurio
• Vasospasmi
• Rekanalisaatio
• Sokeutuminen, kuulon heikkeneminen ja hajuaistin heikkeneminen
• Vierasesinereaktiot, jotka edellyttävät lääketieteellistä interventiota
• Infektiot, jotka edellyttävät lääketieteellistä interventiota
• Katetrointiin
liittyvät
komplikaatiot
(esim.
hematooma
sisäänmenokohdassa, hyytymän muodostuminen katetrin kärkeen ja
tämän jälkeinen paikaltaan pois siirtyminen sekä hermo- ja/tai
verenkiertovauriot, jotka voivat johtaa jalkavammaan)
• Allergiset reaktiot lääkkeille (esim. analgeeteille)
• Allergiset reaktiot non-ionisille varjoaineille tai embolusmateriaalille
• Verisuonen tai leesion repeämä ja verenvuoto
• Kuolema
• Lisätietoja on kohdassa Varoitukset
TURPOAMINEN:
HepaSphere-mikropallot turpoavat, kun ne sekoitetaan käyttövalmiiksi
0,9-prosenttiseen NaCl-vesiliuokseen ja non-ionisiin varjoaineisiin. Kun
HepaSphere-mikropallot hydratoidaan pelkässä 0,9-prosenttisessa
NaCl-vesiliuoksessa tai pelkässä non-ionisessa varjoaineessa tai
yhdistelmässä jossa on 50 % non-ionista varjoainetta ja 50 % 0,9-
prosenttista NaCl-vesiliuosta, ne turpoavat noin nelinkertaisiksi
alkuperäiseen kuivan olomuodon läpimittaan verrattuna noin 10
minuutin kuluessa. Esimerkiksi kuivassa olomuodossaan noin 50–100
mikronia läpimitaltaan olevat HepaSphere-mikropallot turpoavat noin
200–400 mikronin kokoisiksi, kun ne sekoitetaan yllä suositellulla tavalla
käyttövalmiiksi. Turpoamisprosessin luontaisen vaihtelevuuden takia
joidenkin HepaSphere-mikropallojen koko on hieman tämän
vaihteluvälin ulkopuolella käyttövalmiiksi sekoittamisen jälkeen.
Lääkärin täytyy siten valita HepaSphere-mikropallojen koko huolellisesti
kohdesuonten koon ja verisuoniston toivotun okkluusiotason mukaan
sekä vesiliuoksen luonteen mukaisesti.
Huomautus: Jotta HepaSphere-mikropallot turpoavat asianmukaisesti,
ne täytyy altistaa vähintään 10 ml:lle liuosta.
Doksorubisiini-HCl:lla lastattujen mikropallojen turpoamisen voimakkuus
riippuu lastatun lääkeaineen määrästä. HepaSphere-mikropallojen koko
pienenee hieman, noin 20 %, doksorubisiini-HCl:lla lastattuina verrattuna
niiden kokoon pelkässä
0,9-prosenttisessa NaCl-vesiliuoksessa.
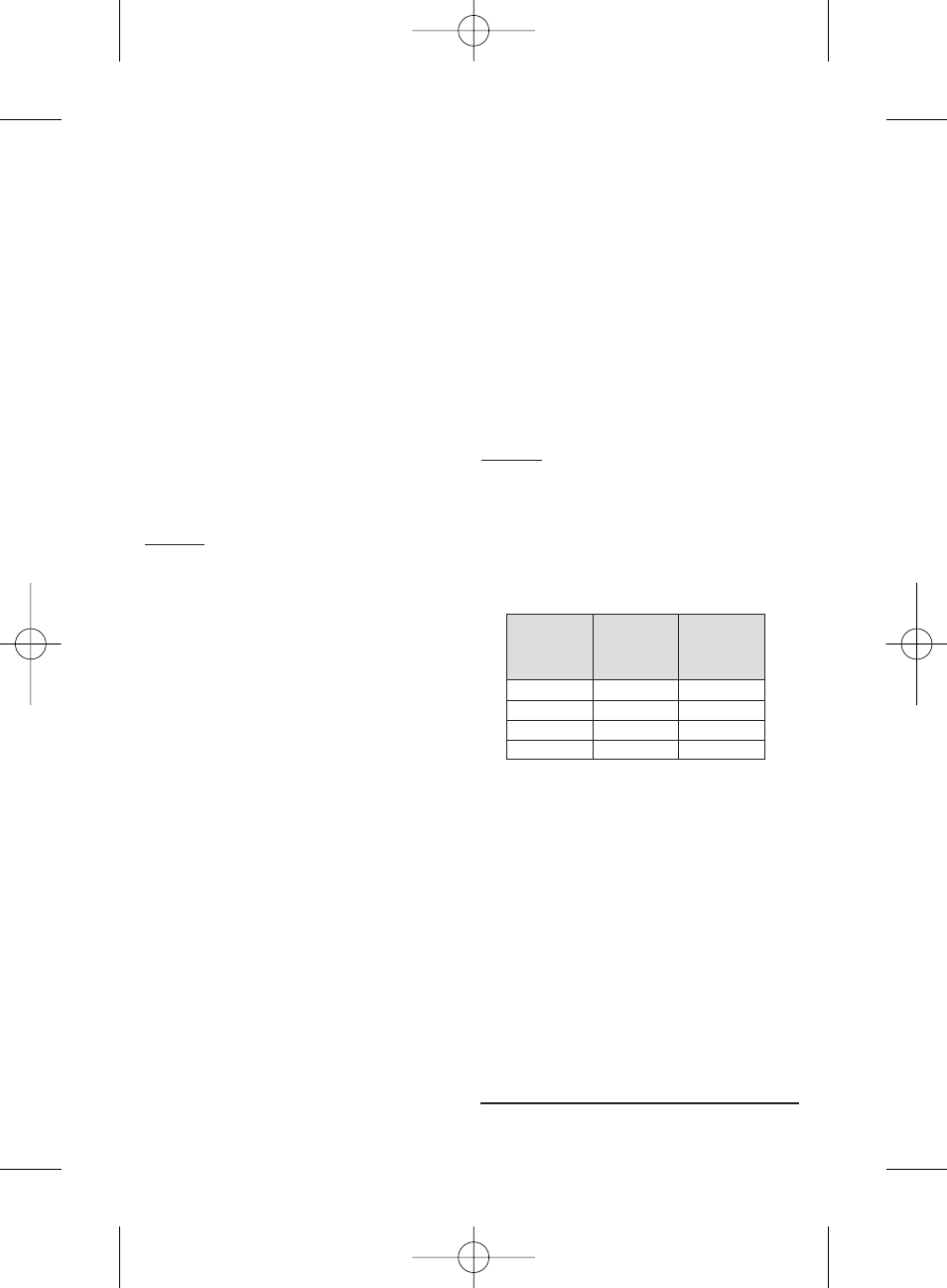
YHTEENSOPIVUUS KATETRIN KANSSA:
HepaSphere-mikropallot voidaan injisoida seuraavan kokoisilla
mikrokatetreilla:
OHJEET:
HepaSphere-mikropallot täytyy sekoittaa käyttövalmiiksi pelkkään 0,9-
prosenttiseen
NaCl-vesiliuokseen
tai
pelkkään
non-ioniseen
varjoaineeseen tai yhdistelmään, josta 50 % on non-ionista varjoainetta
ja 50 % 0,9-prosenttista NaCl-vesiliuosta, jos niitä käytetään ilman
doksorubisiini-HCl:n kuljettamista. Mahdollinen doksorubisiini-HCl-liuos
täytyy lastata ennen katetrin asettamista.
• Valitse HepaSphere-mikropallojen koko tarkasti kohdesuonten koon ja
verisuoniston toivotun okkluusiotason mukaan ja vesiliuoksen luonteen
mukaisesti. Katso kohta "TURPOAMINEN".
• HepaSphere-mikropalloja saattaa olla pullon ulkopuolella. Tästä
johtuen pulloa täytyy käsitellä aseptisesti etäällä pääasialliselta
steriilialueelta.
• Varmista HepaSphere-mikropallojen yhteensopivuus käytettävän
katetrin koon kanssa. Katso edellä oleva taulukko.
• Tarkasta pakkaus sen varmistamiseksi, että se on ehjä. Ota pullo pois
pussista. Pullon ulkopinta on steriili.
HEPASPHERE-MIKROPALLOJA VOIDAAN KÄYTTÄÄ SEKÄ
DOKSORUBISIINI-HCL:LLA
LASTATTUINA
ETTÄ
LASTAAMATTOMINA.
40
Kuiva (µm)
Likimääräinen
kokoalue
käyttövalmiiksi
sekoitettuna (
µm)
Katetrin koko,
sisämitta
(tuumaa)
30-60
120 - 240
≥ 0.021
50-100
200 - 400
≥ 0.021
100-150
400 - 600
≥ 0.024
150-200
600 - 800
≥ 0.027
730095003_A ID 102412_IFU HS DOXO :print 9/11/12 17:10 Page 40
