Merit Medical HepaSphere Microspheres(With Doxorubicin) IFU-Int'l User Manual
Page 12
12
Beutel beschädigt.
Nur für den Gebrauch an einem einzigen Patienten – Packungsinhalt
steril – Den Inhalt einer bereits geöffneten Ampulle nicht erneut
verwenden, wiederaufbereiten oder erneut sterilisieren. Eine erneute
Verwendung oder Sterilisierung bzw. eine Wiederaufbereitung kann die
strukturelle Integrität des Medizinprodukts beeinträchtigen und/oder zu
dessen Versagen führen, was wiederum zu einer Verletzung, Erkrankung
oder zum Tod des Patienten führen kann. Durch eine erneute
Verwendung oder Sterilisierung bzw. eine Wiederaufbereitung kann das
Medizinprodukt auch kontaminiert werden und/oder eine Infektion des
Patienten oder eine Kreuzinfektion einschließlich, aber nicht
ausschließlich, der Übertragung infektiöser Erkrankungen von einem
Patienten zum nächsten bewirken. Eine Kontaminierung des
Medizinprodukts kann zu einer Verletzung, Erkrankung oder zum Tod des
Patienten führen. Alle Prozeduren sind gemäß der validierten
aseptischen Technik durchzuführen.
HepaSphere Mikrosphären DÜRFEN NICHT in ihrem
ursprünglichen trockenen Zustand verwendet werden. Sie
müssen vor Gebrauch gelöst werden. HepaSphere Mikrosphären quellen
in wässriger Lösung auf. Das Ausmaß des Quellvorgangs hängt von der
Ionenkonzentration der Lösung ab. Die Mikrosphären quellen in 0,9%-
iger wässriger Kochsalzlösung und in nicht-ionischen Kontrastlösungen
auf etwa das Vierfache ihres ursprünglichen Durchmessers im trockenen
Zustand. Das Ausmaß des Quellvorgangs bei Beladung mit Doxorubicin-
HCl hängt von der Arzneimittelmenge ab, mit dem das Produkt beladen
wird.
Lyophilisiertes
Doxorubicin-HCl
muss
mit
0,9%-iger
Kochsalzlösung gelöst werden. HepaSphere Mikrosphären quellen bei
Beladung mit Doxorubicin-HCl-Lösung um etwa 20% weniger im
Vergleich zur Auflösung in reiner 0,9%-iger Kochsalzlösung an.
HepaSphere Mikrosphären sind kompressibel und können durch
Mikrokatheter injiziert werden. Allerdings kann die Injektion nicht
vollständig ausgedehnter HepaSphere Mikrosphären dazu führen, dass
das vorgesehene Embolisierungsziel nicht erreicht wird, und dass
möglicherweise ein größerer Gewebebereich embolisiert wird.
Anmerkung: Die maximale empfohlene Konzentration von Doxorubicin-
HCl ist 5 mg/ml. Eine Doxorubicin-HCl-Konzentration höher als 5 mg/ml
erhöht die Viskosität der Lösung wesentlich und erschwert den Umgang
mit HepaSphere Mikrosphären.
Patienten mit bekannten Allergien gegen nicht-ionische Kontrastmittel
benötigen möglicherweise vor Beginn der Embolisierung Kortikosteroide.
Bei Patienten mit folgenden Indikationen können zusätzliche
Untersuchungen und Maßnahmen zur periprozeduralen Therapie
notwendig sein:
• Blutungsdiathese oder hyperkoagulativer Zustand
• mmunschwäche
POTENZIELLE KOMPLIKATIONEN:
Vaskuläre Embolisierung ist ein Verfahren mit hohem Risiko.
Komplikationen können jederzeit während oder nach dem Vorgang
auftreten, darunter u.a. folgende Komplikationen:
• Lähmung aufgrund von ungezielter Embolisierung oder ischämische
Verletzung von benachbarten Gewebeödemen
• Unerwünschter Rückfluss oder Durchgang der HepaSphere
Mikrosphären in normale Arterien in der Nähe der behandelten Läsion,
oder durch die Läsion hindurch in andere Arterien oder arterielle Betten,
wie zum Beispiel in die Arteria carotis interna, in den pulmonalen oder
den koronaren Kreislauf
• Lungenembolie aufgrund von arteriovenösem Shunt
• Ischämie an unerwünschter Stelle, einschließlich Schlaganfall,
ischämischer Infarkt (einschließlich Herzinfarkt) und Gewebenekrose
• Okklusion des Kapillarbetts und Gewebeschaden
• Vasospasmus
• Rekanalisierung
• Erblindung, Hörverlust, Verlust des Geruchssinns
• Abstoßungsreaktionen, die einen medizinischen Eingriff erfordern
• Infektion, die einen medizinischen Eingriff erfordert
• Komplikationen im Zusammenhang mit der Katheterisierung (z.B.
Hämatome an der Eintrittstelle, Gerinnselbildung an der Katheterspitze
und nachfolgende Verlagerung, Nerven- und/oder Kreislaufprobleme, die
zu Beinschädigungen führen können)
• Allergische Reaktion auf die Medikationen (z.B. Analgetika)
• Allergische Reaktion auf nicht-ionische Kontrastmittel oder
embolisches Material
• Gefäß- oder Läsionsriss und Hämorrhagie
• Tod
• Weitere Informationen befinden sich unter „Warnungen“
QUELLVERHALTEN:
HepaSphere Mikrosphären quellen bei Rekonstitution mit 0,9%-iger
wässriger Kochsalzlösung und mit nicht-ionischen Kontrastmitteln auf.
Werden sie mit reiner 0,9%-iger wässriger Kochsalzlösung, 100%-igem
nicht-ionischem Kontrastmittel oder mit einer Mischung angesetzt, die
zur Hälfte aus nicht-ionischem Kontrastmittel und zur Hälfte aus 0,9%-
iger wässriger Kochsalzlösung besteht, quellen HepaSphere
Mikrosphären in etwa 10 Minuten zu ungefähr dem Vierfachen ihres
Originaldurchmessers im trockenen Zustand auf. Zum Beispiel
schwellen HepaSphere Mikrosphären mit einem Trockendurchmesser
von ca. 50-100 Mikron auf etwa 200-400 Mikron an, wenn sie wie unten
empfohlen angesetzt werden.
Wegen der dem Schwellvorgang innewohnenden Variabilität werden
einige der HepaSphere Mikrosphären nach der Rekonstitution leicht
außerhalb dieses Bereiches liegen, sodass der Arzt sicher sein sollte,
sorgfältig die richtige Größe der HepaSphere Mikrosphären im Einklang
mit der Größe der Zielgefäße, mit dem gewünschten Okklusionsniveau
der Gefäßversorgung und mit der Art der wässrigen Lösung zu wählen.
Anmerkung: Damit die HepaSphere Mikrosphären korrekt quellen,
müssen sie in mindestens 10 ml Lösung gegeben werden.
Das Ausmaß des Quellvorgangs bei Beladung mit Doxorubicin-HCl hängt
von der Arzneimittelmenge ab, mit dem das Produkt beladen wird.
HepaSphere Mikrosphären quellen bei Beladung mit Doxorubicin-HCl-
Lösung um etwa 20% weniger im Vergleich zur Auflösung in reiner
0,9%-iger Kochsalzlösung.
KOMPATIBILITÄT DES KATHETERS:
HepaSphere Mikrosphären können mit Mikrokathedern injiziert werden,
die folgende Eigenschaften haben:
ANLEITUNG:
HepaSphere Mikrosphären müssen mit reiner 0,9%-iger wässriger
Kochsalzlösung, 100%-igem nicht-ionischem Kontrastmittel oder mit
einer Mischung gelöst werden, die zur Hälfte aus nicht-ionischem
Kontrastmittel und zur Hälfte aus 0,9%-iger wässriger Kochsalzlösung
besteht, wenn sie ohne Gabe von Doxorubicin-HCl verwendet werden.
Ansonsten müssen sie vor der Positionierung des Katheters mit einer
Doxorubicin-HCl-Lösung beladen werden.
• Wählen Sie die Größe der HepaSphere Mikrosphären sorgfältig mit
Blick auf die Größe der Zielgefäße beim gewünschten Okklusionsniveau
der Gefäßversorgung und die Natur der wässrigen Lösung. Lesen Sie die
Beschreibung des „QUELLVERHALTENS“.
• Es könnten sich HepaSphere Mikrosphären außerhalb der Ampulle
befinden. Deshalb muss die aseptische Handhabung der Ampulle
außerhalb des hauptsächlichen sterilen Bereichs stattfinden.
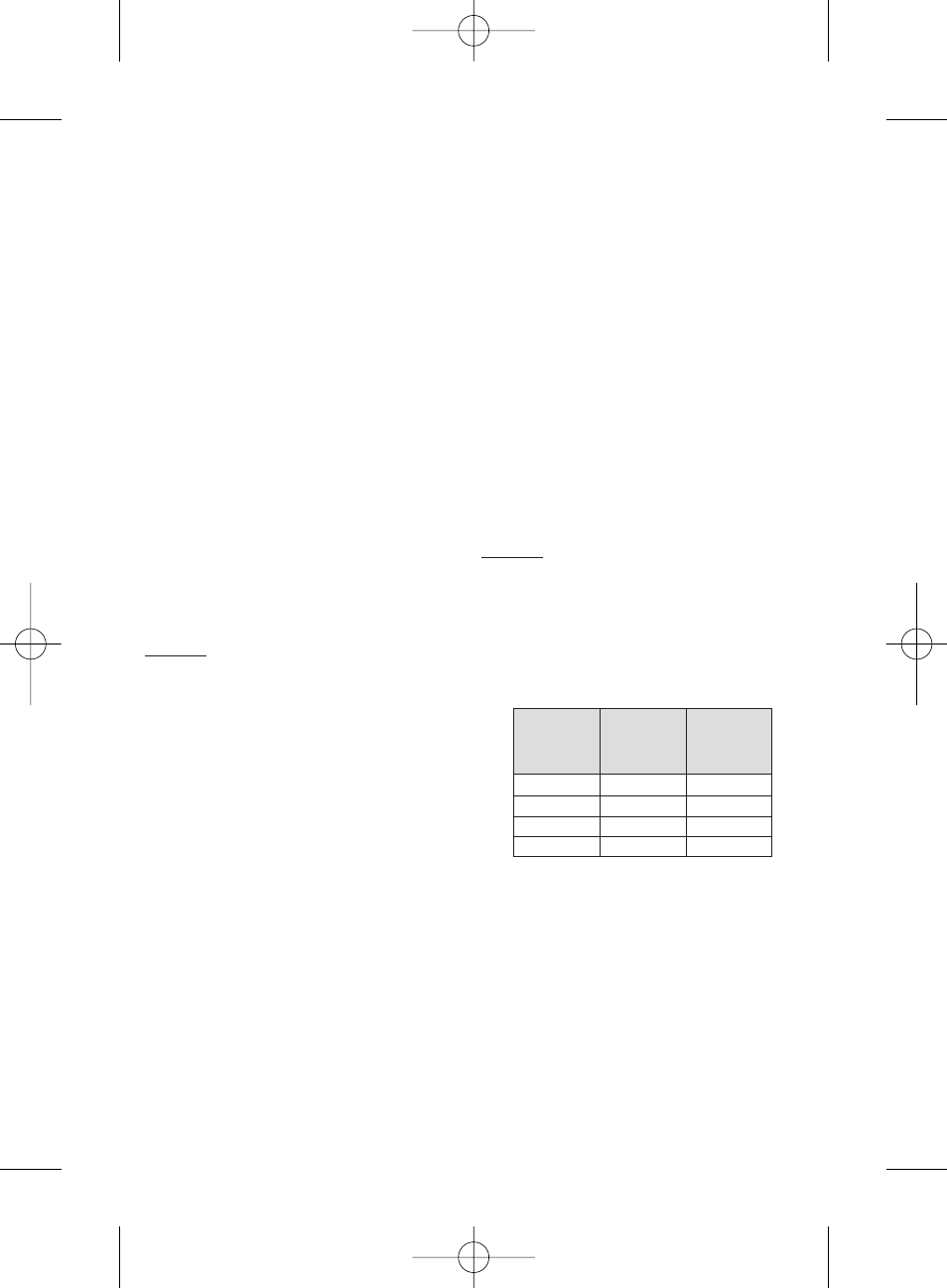
• Stellen Sie sicher, dass die Größe der HepaSphere Mikrosphären mit
der geplanten Größe des zu verwendenden Katheters vereinbar ist. Siehe
Tabelle oben.
Trocken (µm)
Ungefährer
Größenbereich nach
Rekonstitution
(
µm)
Katheter-
größe
ID (in.)
30-60
120 - 240
≥ 0.021
50-100
200 - 400
≥ 0.021
100-150
400 - 600
≥ 0.024
150-200
600 - 800
≥ 0.027
730095003_A ID 102412_IFU HS DOXO :print 9/11/12 17:08 Page 12
